Гібридизація NO2
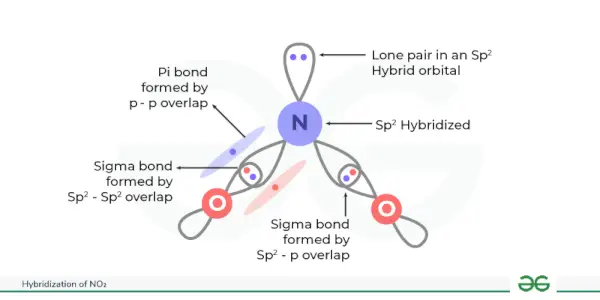
Гібридизація NO 2 є зр 2 . Три еквівалентні гібридні орбіталі створюються під час гібридизації NO 2 . Діоксид азоту, або NO 2 складається з двох атомів кисню в поєднанні з одним атомом нітрогену. Гібридизація NO 2 корисно вивчити розташування атомних орбіталей і його вплив на молекулярну структуру та характеристики.
У цій статті ми розглянемо ідею гібридизації та надамо чітке та зрозуміле пояснення гібридизації NO 2 поряд з гібридизацією обох його іонів NO 2 + і НІ 2 – .
Зміст
- Діоксид азоту [NO2]
- Що таке гібридизація діоксиду азоту (NO2)?
- Гібридизація NO2+ і NO2-
- Гібридизація NO2: поширені запитання
Що таке гібридизація?
Гібридизація в хімії — це процес об’єднання атомних орбіталей для створення нових гібридних орбіталей, які впливають на молекулярну геометрію сполуки та характеристики зв’язку.
Різні типи гібридизації:
- sp Гібридизація
- зр 2 Гібридизація
- зр 3 Гібридизація
Читати далі, Гібридизація .
Що таке гібридизація діоксиду азоту (NO 2 )?
Гібридизація NO 2 є зр 2 .
У цій гібридизації створюються три еквівалентні гібридні орбіталі. Тут азот є центральним атомом, зв’язаним з двома атомами кисню. Нітроген має 5 валентних електронів, розташованих у 2s 2 2п. Тепер один електрон 2s-орбіталі та два електрони 2p-орбіталі брали участь у гібридизації NO 2 таким чином утворюється всього три гібридні орбіталі (1 + 2 = 3), що дає sp 2 гібридизація NO 2 .
Сигма-зв’язки утворюються, коли ці гібридні орбіталі перекриваються з орбіталями кисню, а р-орбіталь атома азоту утворює пі-зв’язок з атомом кисню.

Діоксид азоту [NO 2 ]
Діоксид азоту утворюється, коли два атоми кисню та один атом азоту поєднуються і утворюють двоатомну молекулу NO 2 . Це червонувато-коричневий газ, який має виразний вигляд і різкий їдкий запах. При кімнатній температурі це газ, який демонструє зігнуту або V-подібну молекулярну геометрію.
Крім того, НІ 2 є важливою темою для досліджень у хімічному та екологічному контекстах, оскільки вона впливає на забруднення повітря та хімію атмосфери.
Властивості NO 2
Важливі характеристики NO 2 перераховані нижче:
| Власність | опис |
|---|---|
| Хімічна формула | НІ 2 |
| Молекулярна структура | Вигнуті або V-подібні |
| Стан при кімнатній температурі | газ |
| Колір | Червонувато-коричневий |
| Запах | Гостра, кусуча |
| Точка плавлення | −11,2 °C |
| Точка кипіння | 21,2 °C |
Структура Льюїса NO 2
Детальний опис структури Льюїса NO 2 молекула наведена нижче:
- Азот утворює подвійний зв’язок з одним киснем і п’ятьма валентними електронами, розділяючи два електрони між двома елементами.
- Один електрон вносить другий кисень, оскільки він утворює одинарний зв’язок.
- Одна неподілена пара утримується атомом азоту.
- З азотом як центральним атомом і негативним зарядом (NO 2 – ) на всій молекулі ця конфігурація призводить до лінійної структури.

Детальніше,
- Діоксид азоту
- Оксиди Нітрогену
Валентний кут і геометрія при гібридизації NO 2
Молекулярна геометрія NO 2 стає зігнутою або V-подібною в результаті гібридизації. Атом Нітрогену зазнає sp 2 гібридизація, яка призводить до цієї конфігурації. Атоми Нітрогену та Оксигену утворюють зв’язковий кут, який дорівнює приблизно 134 градуси . Розташування гібридних орбіталей призводить до цього спотвореного кута зв’язку, що додає діоксид азоту (NO 2 ) відмінна структура та характеристики.
Гібридизація NO 2 + і НІ 2 –
Гібридизації НІ 2 + і НІ 2 – обговорюється нижче:
Гібридизація іонів азоту [NO 2 + ]
Гібридизація NO 2 + полягає в наступному:
- Позитивний заряд присутній в іоні азоту (NO 2 + ).
- В НІ 2 + , два атоми кисню та один атом азоту зв’язані між собою.
- Щоб створити дві sp-гібридні орбіталі, атом азоту проходить sp-гібридизацію.
- Для утворення двох сигма-зв’язків ці sp-гібридні орбіталі перекриваються з p-орбіталями кисню.
- Геометрія молекули лінійна.
- Нижче наведено представлення гібридизації: N(sp) + O(p) + O(p).
Гібридизація іонного нітрату [NO 2 – ]
Гібридизація NO 2 – полягає в наступному:
- Негативний заряд присутній в нітрит-іонах (NO 2 – ).
- В НІ 2 – , два атоми кисню та один атом азоту зв’язані між собою.
- Для створення трьох зр 2 гібридних орбіталей, атом Нітрогену проходить через sp 2 гібридизація.
- Щоб утворити три сигма-зв'язки, ці sp 2 гібридні орбіталі перекриваються з р-орбіталями кисню.
- Геометрія молекули тригонально-плоска.
- Нижче представлено гібридизацію: N(sp 2 ) + O(p) + O(p).
Висновок
На завершення дізнайтеся більше про NO 2 Гібридизація відкриває важливі нові погляди на структуру та характеристики молекули. На загальну геометрію впливає азот sp 2 гібридизація, яка дає зігнуту або V-подібну молекулу з кутом зв’язку близько 134 градусів. Унікальні властивості NO 2 частково пояснюються нерівною довжиною зв’язків N-O.
| Аспект | опис |
|---|---|
| Гібридизація | НІ 2 зазнає sp 2 гібридизація |
| Молекулярна геометрія | Вигнуті або V-подібні |
| Кут зв'язку | Приблизно 134 градуси між азотом і киснем |
| Спотворення довжини зв'язку | Нерівні довжини зв’язків через sp 2 гібридизація |
Також перевірте, Гібридизація SF 4
Гібридизація NO 2 : поширені запитання
1. Як діє НІ 2 Впливають на довкілля?
Одним із основних забруднювачів повітря є NO 2 , що впливає як на екосистему, так і на здоров’я людини, викликаючи проблеми з диханням і кислотні дощі.
2. Який кут сполучення більший серед NO 2 + або ні 2 ?
Тоді як НІ 2 має менший зв’язувальний кут із sp2-гібридизацією та тригональну планарну структуру, NO2+ має ширший зв’язувальний кут, оскільки він проходить через sp-гібридизацію з лінійною геометрією.
3. Що таке геометрія NO 2 ?
Структура НІ 2 молекула зігнута, або V-подібна.
4. Що таке молекулярна геометрія NO 2 + ?
Геометрія NO 2 + молекул є лінійним.
5. Яка кількість сигма- та пі-зв’язків є в NO₂?
NO₂ має один сигма-зв’язок і один пі-зв’язок.
6. NO₂ полярний чи неполярний?
NO₂ є полярною частинкою через наявність самотньої пари на азоті та викривлену субатомну розрахунку, яка спонукає до однобічної циркуляції заряду.
7. Що таке валентний кут у NO₂?
Вагонний кут в НІ 2 становить приблизно 134 градуси.