NO2 hibridizācija
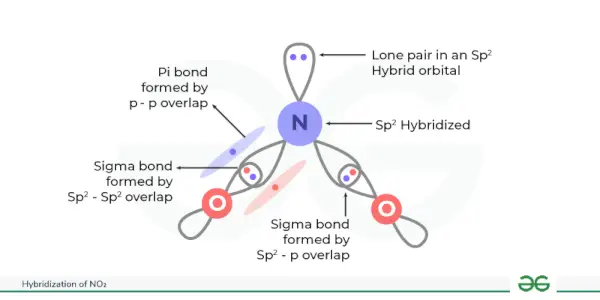
NO hibridizācija 2 ir sp 2 . NO hibridizācijā tiek izveidotas trīs līdzvērtīgas hibrīda orbitāles 2 . Slāpekļa dioksīds jeb NO 2 sastāv no diviem skābekļa atomiem, kas apvienoti ar vienu slāpekļa atomu. NO hibridizācija 2 ir lietderīgi izpētīt atomu orbitāļu izvietojumu un tā ietekmi uz to molekulāro struktūru un īpašībām.
Šajā rakstā mēs izpētīsim hibridizācijas ideju un sniegsim skaidru un saprotamu NO hibridizācijas skaidrojumu 2 kopā ar abu tā jonu hibridizāciju NO 2 + un NĒ 2 – .
Satura rādītājs
- Slāpekļa dioksīds [NO2]
- Kas ir slāpekļa dioksīda (NO2) hibridizācija?
- NO2+ un NO2- hibridizācija
- NO2 hibridizācija: FAQ
Kas ir hibridizācija?
Hibridizācija ķīmijā ir atomu orbitāļu apvienošanas process, lai izveidotu jaunas hibrīda orbitāles, kas ietekmē savienojuma molekulāro ģeometriju un savienojuma īpašības.
Ir dažādi hibridizācijas veidi:
- sp Hibridizācija
- sp 2 Hibridizācija
- sp 3 Hibridizācija
Lasīt vairāk, Hibridizācija .
Kas ir slāpekļa dioksīda hibridizācija (NO 2 )?
NO hibridizācija 2 ir sp 2 .
Šajā hibridizācijā tiek izveidotas trīs līdzvērtīgas hibrīda orbitāles. Šeit slāpeklis ir centrālais atoms, kas saistīts ar diviem skābekļa atomiem. Slāpeklī ir 5 valences elektroni, kas sakārtoti 2s 2 2p. Tagad viens 2s orbitāles elektrons un divi elektroni 2p orbitālē piedalījās NO hibridizācijā 2 tādējādi kopumā veidojas trīs hibrīdorbitāles (1 + 2 = 3), kas dod sp 2 NO hibridizācija 2 .
Sigmas saites rodas, kad šīs hibrīdās orbitāles pārklājas ar skābekļa orbitālēm, un slāpekļa atoma p orbitāle veido pi saiti ar skābekļa atomu.

Slāpekļa dioksīds [NO 2 ]
Slāpekļa dioksīds rodas, apvienojot divus skābekļa atomus un vienu slāpekļa atomu un veido divatomu molekulu NO 2 . Tā ir sarkanbrūna gāze, kurai ir izteikts izskats un asa, kodīga smaka. Istabas temperatūrā tā ir gāze, kurai ir izliekta vai V-veida molekulārā ģeometrija.
Turklāt NĒ 2 ir svarīgs pētniecības temats ķīmiskajā un vides kontekstā, jo tas ietekmē gaisa piesārņojumu un atmosfēras ķīmiju.
Īpašības NO 2
Svarīgās NO īpašības 2 ir uzskaitīti zemāk:
| Īpašums | Apraksts |
|---|---|
| Ķīmiskā formula | NĒ 2 |
| Molekulārā struktūra | Liekts vai V-veida |
| Stāvoklis istabas temperatūrā | Gāze |
| Krāsa | Sarkanbrūns |
| Smarža | Ass, kodīgs |
| Kušanas punkts | −11,2 °C |
| Vārīšanās punkts | 21,2 °C |
Lūisa struktūra NO 2
Sīks Lūisa struktūras apraksts NO 2 molekula ir dota zemāk:
- Slāpeklis veido dubultsaiti ar vienu skābekli un pieciem valences elektroniem, sadalot divus elektronus starp diviem elementiem.
- Viens elektrons tiek pievienots otrajam skābeklim, jo tas veido vienotu saiti.
- Slāpekļa atoms saglabā vienu vientuļo pāri.
- Ar slāpekli kā centrālo atomu un negatīvu lādiņu (NO 2 – ) visā molekulā, šī konfigurācija rada lineāru struktūru.

Lasīt vairāk,
- Slāpekļa dioksīds
- Slāpekļa oksīdi
Saites leņķis un ģeometrija NO hibridizācijā 2
NO molekulārā ģeometrija 2 hibridizācijas rezultātā kļūst saliekta vai V-veida. Slāpekļa atoms iziet sp 2 hibridizācija, kas rada šo konfigurāciju. Slāpekļa un skābekļa atomi veido saiknes leņķi, kas ir aptuveni 134 grādi . Hibrīdu orbitāļu izvietojums rada šo deformēto saites leņķi, kas palielina slāpekļa dioksīdu (NO 2 ) atšķirīga struktūra un īpašības.
NO hibridizācija 2 + un NĒ 2 –
Hibridizācija ir NO 2 + un NĒ 2 – apspriests zemāk:
Slāpekļa jonu hibridizācija[NO 2 + ]
NO hibridizācija 2 + ir šāds:
- Slāpekļa jonā ir pozitīvs lādiņš (NO 2 + ).
- In NO 2 + , divi skābekļa atomi un viens slāpekļa atoms ir saistīti kopā.
- Lai izveidotu divas sp hibrīda orbitāles, slāpekļa atoms iziet sp hibridizāciju.
- Lai izveidotu divas sigma saites, šīs sp hibrīda orbitāles pārklājas ar skābekļa p orbitālēm.
- Molekulas ģeometrija ir lineāra.
- Tālāk ir parādīts hibridizācijas attēlojums: N(sp) + O(p) + O(p).
Jonu nitrāta hibridizācija [NO 2 – ]
NO hibridizācija 2 – ir šāds:
- Nitrītu jonos ir negatīvs lādiņš (NO 2 – ).
- In NO 2 – , divi skābekļa atomi un viens slāpekļa atoms ir saistīti kopā.
- Lai izveidotu trīs sp 2 hibrīda orbitāles, slāpekļa atoms iet caur sp 2 hibridizācija.
- Lai izveidotu trīs sigma saites, šīs sp 2 hibrīda orbitāles pārklājas ar skābekļa p orbitālēm.
- Molekulas ģeometrija ir plakana trigonāli.
- Sekojošais attēlo hibridizāciju: N (sp 2 ) + O(p) + O(p).
Secinājums
Noslēgumā, uzzinot vairāk par NO 2 Hibridizācija piedāvā svarīgas jaunas perspektīvas par molekulas uzbūvi un īpašībām. Kopējo ģeometriju ietekmē slāpekļa sp 2 hibridizācija, kas dod saliektu vai V-veida molekulu ar saites leņķi aptuveni 134 grādi. NO unikālās īpašības 2 daļēji ir saistīti ar nevienlīdzīgajiem saišu garumiem N-O saitēs.
| Aspekts | Apraksts |
|---|---|
| Hibridizācija | NĒ 2 iziet sp 2 hibridizācija |
| Molekulārā ģeometrija | Liekts vai V-veida |
| Saites leņķis | Aptuveni 134 grādi starp slāpekli un skābekli |
| Saites garuma kropļojumi | Nevienlīdzīgi saišu garumi sp 2 hibridizācija |
Pārbaudiet arī, SF hibridizācija 4
NO hibridizācija 2 : FAQ
1. Kā NĒ 2 Ietekmē vidi?
Viens no galvenajiem gaisa piesārņotājiem ir NĒ 2 , kas ietekmē gan ekosistēmu, gan cilvēku veselību, izraisot elpošanas problēmas un skābos lietus.
2. Kurš saites leņķis ir lielāks starp NO 2 + vai nē 2 ?
Tā kā NĒ 2 ir mazāks saites leņķis ar sp2 hibridizāciju un trigonālu plakanu struktūru, NO2+ ir plašāks saites leņķis, jo tas iet caur sp hibridizāciju ar lineāro ģeometriju.
3. Kāda ir NO ģeometrija 2 ?
NĒ struktūra 2 molekula ir saliekta vai V-veida.
4. Kāda ir NO molekulārā ģeometrija 2 + ?
NO ģeometrija 2 + molekulas ir lineāras.
5. Cik sigma un pi saišu ir NO₂?
NO₂ ir viena sigma saite un viena pi saite.
6. Vai NO₂ ir polārs vai nepolārs?
NO₂ ir polāra daļiņa, jo uz slāpekļa atrodas vientuļš pāris un izliekts subatomu aprēķins, kas izraisa nelīdzenu lādiņa cirkulāciju.
7. Kāds ir saites leņķis NO₂?
Saites leņķis NO 2 ir aptuveni 134 grādi.