Ibridazione di NO2
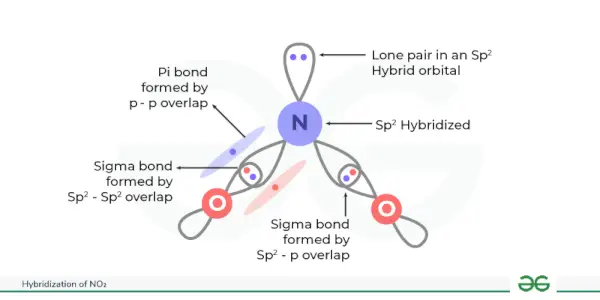
Ibridazione di NO 2 è sp 2 . Tre orbitali ibridi equivalenti vengono creati nell'ibridazione di NO 2 . Biossido di azoto o NO 2 è costituito da due atomi di ossigeno combinati con un atomo di azoto. Ibridazione di NO 2 è utile esaminare la disposizione degli orbitali atomici e il suo effetto sulla sua struttura e caratteristiche molecolari.
In questo articolo esploreremo l'idea di ibridazione e forniremo una spiegazione chiara e comprensibile dell'ibridazione di NO 2 insieme all'ibridazione di entrambi i suoi ioni NO 2 + e NO 2 – .
Tabella dei contenuti
- Biossido di azoto[NO2]
- Cos'è l'ibridazione del biossido di azoto (NO2)?
- Ibridazione di NO2+ e NO2-
- Ibridazione di NO2: domande frequenti
Cos'è l'ibridazione?
L’ibridazione, in chimica, è il processo di combinazione degli orbitali atomici per creare nuovi orbitali ibridi che influenzano la geometria molecolare e le caratteristiche di legame di un composto.
Diversi tipi di ibridazione sono:
- sp Ibridazione
- sp 2 Ibridazione
- sp 3 Ibridazione
Per saperne di più, Ibridazione .
Cos'è l'ibridazione del biossido di azoto (NO 2 )?
Ibridazione di NO 2 è sp 2 .
In questa ibridazione vengono creati tre orbitali ibridi equivalenti. Qui, l'azoto è l'atomo centrale legato a due atomi di ossigeno. L'azoto ha 5 elettroni di valenza disposti in 2 secondi 2 2p. Ora, l’elettrone dell’orbitale 2s e i due elettroni dell’orbitale 2p hanno partecipato all’ibridazione di NO 2 si formano così tre orbitali ibridi in totale (1 + 2 = 3), dando sp 2 ibridazione di NO 2 .
I legami Sigma vengono creati quando questi orbitali ibridi si sovrappongono agli orbitali dell'ossigeno e l'orbitale p dell'atomo di azoto forma un legame pi con l'atomo di ossigeno.

Biossido di azoto[NO 2 ]
Il biossido di azoto viene creato quando due atomi di ossigeno e un atomo di azoto si combinano e compongono la molecola biatomica NO 2 . È un gas bruno-rossastro che ha un aspetto distinto e un odore acuto e pungente. A temperatura ambiente, è un gas che presenta una geometria molecolare piegata o a forma di V.
Inoltre, NO 2 è un importante argomento di ricerca in contesti chimici e ambientali perché influenza l'inquinamento atmosferico e la chimica atmosferica.
Proprietà del n 2
Le caratteristiche importanti di NO 2 sono elencati di seguito:
| Proprietà | Descrizione |
|---|---|
| Formula chimica | NO 2 |
| Struttura molecolare | Piegato o a forma di V |
| Stato a temperatura ambiente | Gas |
| Colore | Marrone rossastro |
| Odore | Affilato, pungente |
| Punto di fusione | −11,2 °C |
| Punto di ebollizione | 21,2 °C |
Struttura di Lewis del n 2
La descrizione dettagliata della struttura di Lewis di NO 2 la molecola è la seguente:
- L'azoto forma un doppio legame con un ossigeno e cinque elettroni di valenza, condividendo due elettroni tra i due elementi.
- Un elettrone viene fornito dal secondo ossigeno mentre forma un singolo legame.
- Una coppia solitaria è trattenuta dall'atomo di azoto.
- Con l'azoto come atomo centrale e una carica negativa (NO 2 – ) sull'intera molecola, questa configurazione si traduce in una struttura lineare.

Per saperne di più,
- Diossido di azoto
- Ossidi di azoto
Angolo di legame e geometria nell'ibridazione di NO 2
La geometria molecolare di NO 2 diventa piegato o a forma di V a causa dell'ibridazione. L'atomo di azoto subisce sp 2 ibridazione, che porta a questa configurazione. Gli atomi di azoto e ossigeno formano un angolo di legame di circa 134 gradi . La disposizione degli orbitali ibridi risulta in questo angolo di legame distorto, che si aggiunge al biossido di azoto (NO 2 ) struttura e caratteristiche distinte.
Ibridazione di NO 2 + e NO 2 –
L'ibridazione di è NO 2 + e NO 2 – discusso di seguito:
Ibridazione dello ione azoto[NO 2 + ]
L'ibridazione di NO 2 + è come segue:
- Nello ione azoto è presente una carica positiva (NO 2 + ).
- Nel n 2 + , due atomi di ossigeno e un atomo di azoto sono legati insieme.
- Per creare due orbitali ibridi sp, l'atomo di azoto passa attraverso l'ibridazione sp.
- Per formare due legami sigma, questi orbitali ibridi sp si sovrappongono agli orbitali p dell'ossigeno.
- La geometria della molecola è lineare.
- Quella che segue è una rappresentazione dell'ibridazione: N(sp) + O(p) + O(p).
Ibridazione dello ione nitrato [NO 2 – ]
L'ibridazione di NO 2 – è come segue:
- Una carica negativa è presente negli ioni nitrito (NO 2 – ).
- Nel n 2 – , due atomi di ossigeno e un atomo di azoto sono legati insieme.
- Per creare tre sp 2 orbitali ibridi, l'atomo di azoto passa attraverso sp 2 ibridazione.
- Per formare tre legami sigma, questi sp 2 gli orbitali ibridi si sovrappongono agli orbitali p dell'ossigeno.
- La geometria della molecola è trigonale planare.
- Quanto segue rappresenta l'ibridazione: N(sp 2 ) + O(p) + O(p).
Conclusione
In conclusione, saperne di più su NO 2 L’ibridazione offre nuove importanti prospettive sulla composizione e sulle caratteristiche della molecola. La geometria complessiva è influenzata dall'azoto sp 2 ibridazione, che produce una molecola piegata o a forma di V con un angolo di legame di circa 134 gradi. Le proprietà uniche di NO 2 sono in parte attribuiti alle lunghezze disuguali dei legami N-O.
| Aspetto | Descrizione |
|---|---|
| Ibridazione | NO 2 subisce sp 2 ibridazione |
| Geometria Molecolare | Piegato o a forma di V |
| Angolo di legame | Circa 134 gradi tra azoto e ossigeno |
| Distorsione della lunghezza del legame | Lunghezze di legame disuguali dovute a sp 2 ibridazione |
Controlla anche, Ibridazione di SF 4
Ibridazione di NO 2 : Domande frequenti
1. Come funziona il NO 2 Influiscono sull'ambiente?
Uno dei principali inquinanti atmosferici è il NO 2 , che colpisce sia l'ecosistema che la salute umana causando problemi respiratori e piogge acide.
2. Quale angolo di legame è maggiore tra NO 2 + o no 2 ?
Mentre il NO 2 ha un angolo di legame minore con ibridazione sp2 e una struttura planare trigonale, NO2+ ha un angolo di legame più ampio poiché passa attraverso l'ibridazione sp con una geometria lineare.
3. Qual è la geometria di NO 2 ?
La struttura del n 2 la molecola è piegata o a forma di V.
4. Qual è la geometria molecolare di NO 2 + ?
La geometria del n 2 + molecole è lineare.
5. Quanti legami Sigma e pi sono presenti nell'NO₂?
NO₂ ha un legame sigma e un legame pi greco.
6. L'NO₂ è polare o non polare?
NO₂ è una particella polare a causa della presenza di una coppia solitaria sull'azoto e del calcolo subatomico incurvato, che provoca una circolazione sbilanciata della carica.
7. Qual è l'angolo di legame in NO₂?
L'angolo di legame in NO 2 è di circa 134 gradi.