Hibridación de NO2
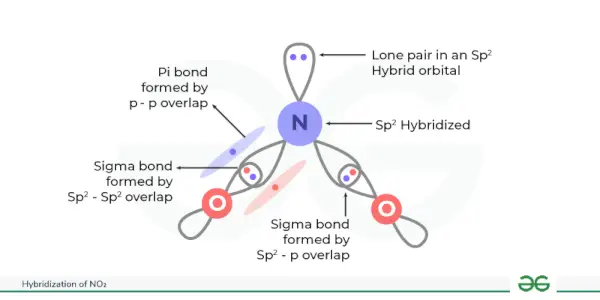
Hibridación de NO 2 es sp 2 . Se crean tres orbitales híbridos equivalentes en la Hibridación del NO 2 . Dióxido de nitrógeno o NO 2 consta de dos átomos de oxígeno combinados con un átomo de nitrógeno. Hibridación de NO 2 Es útil para examinar la disposición de los orbitales atómicos y su efecto sobre su estructura y características moleculares.
En este artículo, exploraremos la idea de hibridación y brindaremos una explicación clara y comprensible de la hibridación del NO. 2 junto con la hibridación de ambos sus iones NO 2 + y no 2 – .
Tabla de contenidos
- Dióxido de nitrógeno[NO2]
- ¿Qué es la hibridación del dióxido de nitrógeno (NO2)?
- Hibridación de NO2+ y NO2-
- Hibridación de NO2: preguntas frecuentes
¿Qué es la hibridación?
La hibridación, en química, es el proceso de combinar orbitales atómicos para crear nuevos orbitales híbridos que afectan la geometría molecular y las características de enlace de un compuesto.
Los diferentes tipos de Hibridación son:
- sp Hibridación
- sp 2 Hibridación
- sp 3 Hibridación
Leer más, Hibridación .
¿Qué es la hibridación del dióxido de nitrógeno (NO? 2 )?
Hibridación de NO 2 es sp 2 .
En esta hibridación se crean tres orbitales híbridos equivalentes. Aquí, el nitrógeno es el átomo central unido a dos átomos de oxígeno. El nitrógeno tiene 5 electrones de valencia dispuestos en 2s. 2 2p. Ahora, el electrón del orbital 2s y dos electrones del orbital 2p participaron en la hibridación del NO. 2 por lo tanto se forman un total de tres orbitales híbridos (1 + 2 = 3), dando sp 2 hibridación de NO 2 .
Los enlaces sigma se crean cuando estos orbitales híbridos se superponen con los orbitales de oxígeno y el orbital p del átomo de nitrógeno forma un enlace pi con el átomo de oxígeno.

Nitrogen Dioxide[NO 2 ]
El dióxido de nitrógeno se crea cuando dos átomos de oxígeno y un átomo de nitrógeno se combinan y forman la molécula diatómica NO. 2 . Es un gas de color marrón rojizo que tiene una apariencia distintiva y un olor penetrante y penetrante. A temperatura ambiente, es un gas que presenta una geometría molecular curvada o en forma de V.
Además, NO 2 Es un tema importante de investigación en contextos químicos y ambientales porque afecta la contaminación del aire y la química atmosférica.
Propiedades del NO 2
Las características importantes del NO 2 están enlistados debajo:
| Propiedad | Descripción |
|---|---|
| Fórmula química | NO 2 |
| Estructura molecular | Doblado o en forma de V |
| Estado a temperatura ambiente | Gas |
| Color | Marrón rojizo |
| Olor | Afilado, mordiente |
| Punto de fusion | −11,2 ºC |
| Punto de ebullición | 21,2 ºC |
Estructura de Lewis del NO 2
La descripción detallada de la estructura de Lewis del NO. 2 molécula se da a continuación:
- El nitrógeno forma un doble enlace con un oxígeno y cinco electrones de valencia, compartiendo dos electrones entre los dos elementos.
- El segundo oxígeno aporta un electrón mientras forma un enlace simple.
- El átomo de nitrógeno retiene un par solitario.
- Con nitrógeno como átomo central y carga negativa (NO 2 – ) en toda la molécula, esta configuración da como resultado una estructura lineal.

Leer más,
- Dioxido de nitrogeno
- Óxido de nitrógeno
Ángulo de enlace y geometría en la hibridación de NO. 2
La geometría molecular del NO 2 se dobla o tiene forma de V como resultado de la hibridación. El átomo de nitrógeno sufre sp 2 hibridación, que da como resultado esta configuración. Los átomos de nitrógeno y oxígeno forman un ángulo de enlace que es aproximadamente 134 grados . La disposición de los orbitales híbridos da como resultado este ángulo de enlace distorsionado, que se suma al dióxido de nitrógeno (NO 2 ) estructura y características distintas.
Hibridación de NO 2 + y no 2 –
La hibridación de es NO. 2 + y no 2 – se discute más adelante:
Hibridación de iones nitrógeno [NO 2 + ]
La hibridación de NO 2 + es como sigue:
- Una carga positiva está presente en el ion nitrógeno (NO 2 + ).
- En NO 2 + , dos átomos de oxígeno y un átomo de nitrógeno están unidos.
- Para crear dos orbitales híbridos sp, el átomo de nitrógeno pasa por una hibridación sp.
- Para formar dos enlaces sigma, estos orbitales híbridos sp se superponen con los orbitales p del oxígeno.
- La geometría de la molécula es lineal.
- La siguiente es una representación de la hibridación: N(sp) + O(p) + O(p).
Hibridación de iones nitrato [NO 2 – ]
La hibridación de NO 2 – es como sigue:
- Una carga negativa está presente en los iones nitrito (NO 2 – ).
- En NO 2 – , dos átomos de oxígeno y un átomo de nitrógeno están unidos.
- Para crear tres sp 2 orbitales híbridos, el átomo de nitrógeno pasa por sp 2 hibridación.
- Para formar tres enlaces sigma, estos sp 2 Los orbitales híbridos se superponen con los orbitales p del oxígeno.
- La geometría de la molécula es plana trigonal.
- Lo siguiente representa la hibridación: N(sp 2 ) + O(p) + O(p).
Conclusión
En conclusión, aprender más sobre el NO 2 La hibridación ofrece nuevas perspectivas importantes sobre la composición y las características de la molécula. La geometría general está influenciada por el nitrógeno sp. 2 hibridación, que produce una molécula doblada o en forma de V con un ángulo de enlace de aproximadamente 134 grados. Las propiedades únicas del NO 2 se atribuyen en parte a las longitudes desiguales de los enlaces en los enlaces N-O.
| Aspecto | Descripción |
|---|---|
| Hibridación | NO 2 se somete a sp 2 hibridación |
| Geometría molecular | Doblado o en forma de V |
| Ángulo de enlace | Aproximadamente 134 grados entre nitrógeno y oxígeno. |
| Distorsión de la longitud del enlace | Longitudes de enlace desiguales debido a sp 2 hibridación |
Compruebe también, Hibridación de SF 4
Hibridación de NO 2 : Preguntas frecuentes
1. ¿Cómo NO? 2 ¿Afecta el medio ambiente?
Uno de los principales contaminantes del aire es el NO. 2 , que afecta tanto al ecosistema como a la salud humana al provocar problemas respiratorios y lluvia ácida.
2. ¿Qué ángulo de enlace es mayor entre NO? 2 + o no 2 ?
Mientras que NO 2 tiene un ángulo de enlace menor con hibridación sp2 y una estructura plana trigonal, el NO2+ tiene un ángulo de enlace más amplio a medida que pasa a través de la hibridación sp con una geometría lineal.
3. ¿Cuál es la geometría del NO? 2 ?
La estructura del NO 2 La molécula está doblada o tiene forma de V.
4. ¿Cuál es la geometría molecular del NO? 2 + ?
La geometría del NO 2 + moléculas es lineal.
5. ¿Qué cantidad de enlaces Sigma y pi hay en el NO₂?
El NO₂ tiene un enlace sigma y un enlace pi.
6. ¿El NO₂ es polar o no polar?
El NO₂ es una partícula polar debido a la presencia de un par solitario en el nitrógeno y al cálculo subatómico arqueado, lo que provoca una circulación desequilibrada de carga.
7. ¿Cuál es el ángulo de enlace en NO₂?
El ángulo de enlace en NO 2 es aproximadamente 134 grados.